Ads Neuropsiquiatría
RITALIN LA
Estás aquí
Contáctanos
Forma Farmacéutica:
Cápsulas
Consideración de uso:
Liberación prolongada
Formulación:
Cada cápsula contiene:
Clorhidrato de metilfenidato 10 mg ó 20 mg ó 30 mg ó 40 mg
Excipiente cbp 1 cápsula
Trastorno del déficit de atención con hiperactividad (TDAH, DSM-IV):
RITALIN® LA está indicada para el tratamiento del TDAH en niños de 6 años o más y en adultos.
El trastorno por déficit de atención con hiperactividad (TDAH), o ADHD (por sus siglas en inglés: Attention Deficit/Hyperactivity Disorder), se conocía anteriormente como <trastorno por déficit de atención> o <disfunción cerebral mínima>. Otros términos empleados para describir este trastorno de la conducta son: síndrome hipercinético, lesión cerebral mínima, disfunción cerebral mínima, disfunción cerebral menor y síndrome psicoorgánico de los pacientes.
RITALIN® LA se indica como parte de un programa integral que incluye medidas psicológicas, pedagógicas y sociales tendientes a estabilizar a los pacientes que presentan un síndrome de trastorno de la conducta caracterizado por una distracción moderada a severa, breves períodos de atención, hiperactividad, inestabilidad emocional, e impulsibilidad.
El diagnóstico se debe efectuar según los criterios del DSM-IV o de los lineamientos de la CIE-10. Pueden presentarse signos neurológicos (leves no localizados, problemas de aprendizaje y EEG anómalo); pero también puede ser que no aparezcan, y el diagnóstico de disfunción del SNC podrá o no ser necesario.
Consideraciones especiales para el diagnóstico del TDAH en niños.
No se conoce la etiología específica de este síndrome ni se dispone de ninguna prueba diagnóstica. Para diagnosticarlo correctamente es necesario realizar un análisis multidisciplinario en el que incluyan las partes médicas, neuropsicológica, pedagógica y social. Las características más comunes del trastorno son: antecedentes de períodos de atención breves, distractibilidad, inestabilidad emocional, impulsividad, hiperactividad moderada o grave, signos neurológicos leves y un EEG anormal. En algunos casos pueden presentarse dificultades del aprendizaje.
El diagnóstico debe basarse en la anamnesis y evaluación completa del niño y no solo en la presencia de una o más de estas características. No todos los niños con este síndrome necesitan tratamiento con fármacos.
Los estimulantes no están indicados en los niños con síntomas inducidos por factores externos (en particular maltrato) y/o trastornos psiquiátricos primarios, incluyendo la psicosis. Es fundamental tratar estos casos en un ámbito pedagógico adecuado, siendo por lo general necesaria la intervención psicosocial. Cuando estas medidas resulten insuficientes, la decisión de prescribir un estimulante dependerá de la evaluación meticulosa de la severidad de los síntomas que presenta el niño.
Consideraciones especiales para el diagnóstico del TDAH en adultos
No se conoce la causa específica de este síndrome, ni se dispone de una prueba diagnóstica única. La sintomatología característica del TDAH en adultos consiste en cambios constantes de actividad, propensión al aburrimiento, agitación, impaciencia y falta de atención. Los síntomas como la hiperactividad tienden a atenuarse con la edad, posiblemente debido a la adaptación, al desarrollo neurológico y a la automedicación.
Los síntomas de falta de atención son predominantes y tienen mayores consecuencias en los adultos con TDAH. Para realizar un diagnóstico correcto en adultos, es preciso identificar los síntomas del paciente mediante una entrevista estructurada. Debe determinarse retrospectivamente si el paciente padece TDAH desde la niñez.
El diagnóstico no debe basarse exclusivamente en la presencia de uno o varios síntomas. La decisión de recetar un estimulante en adultos sólo deberá tomarse tras una evaluación muy completa de la gravedad y del carácter crónico de los síntomas, así como de sus efectos en la vida diaria del paciente.
- Hipersensibilidad al metilfenidato o a cualquiera de los excipientes.
- Ansiedad o angustia, tensión.
- Agitación.
- Hipertiroidismo.
- Desordenes cardiacos pre-existentes los cuales incluyen hipertensión severa, angina de pecho, enfermedad arterial oclusiva, insuficiencia cardiaca, cardiopatías congénitas hemodinámicamente significativas, miocardiopatías, infarto al miocardio, arritmias potencialmente mortales y canalopatías (desordenes causados por la disfunción de los canales iónicos).
- Durante el tratamiento con inhibidores de la monoaminooxidasa (MAO) o en un plazo de un mínimo de 2 semanas después de suspender la administración de dichos fármacos, debido al riesgo de crisis hipertensiva (ver Interacciones medicamentosas y de otro género).
- Glaucoma.
- Feocromocitoma.
- Diagnóstico o antecedentes familiares de Síndrome de Tourette.
El nerviosismo y el insomnio son reacciones adversas muy frecuentes al comienzo del tratamiento con RITALIN® LA, que se pueden controlar con la reducción de la dosis o la omisión de la dosis vespertina o nocturna del medicamento.
La pérdida de apetito es muy frecuente, aunque usualmente pasajera. Son frecuentes a muy frecuentes los dolores abdominales, las náuseas y los vómitos; por lo general ocurren al comienzo del tratamiento y pueden aliviarse mediante la ingestión simultánea de alimentos.
Resumen tabulado de las reacciones adversas
La tabla 1 enumera las reacciones adversas por clases de trastornos del diccionario MedDRA (por sistema u órgano). En cada clase de trastornos, las reacciones adversas se han clasificado en orden decreciente de frecuencia, y en cada categoría de frecuencia se han clasificado en orden decreciente de gravedad. Además, para definir la categoría de frecuencia asignada a cada reacción adversa, se ha empleado la siguiente convención (CIOMS III): muy frecuentes (³ 1/10); frecuentes (³ 1/100 - < 1/10); infrecuentes (³ 1/1000 - < 1/100); raras (³ 1/10.000 - < 1/1000); muy raras (< 1/10.000).
Tabla 1 Efectos adversos reportados con el uso de RITALIN® LA de los estudios clínicos, la farmacovigilancia y los casos reportados en la literatura.
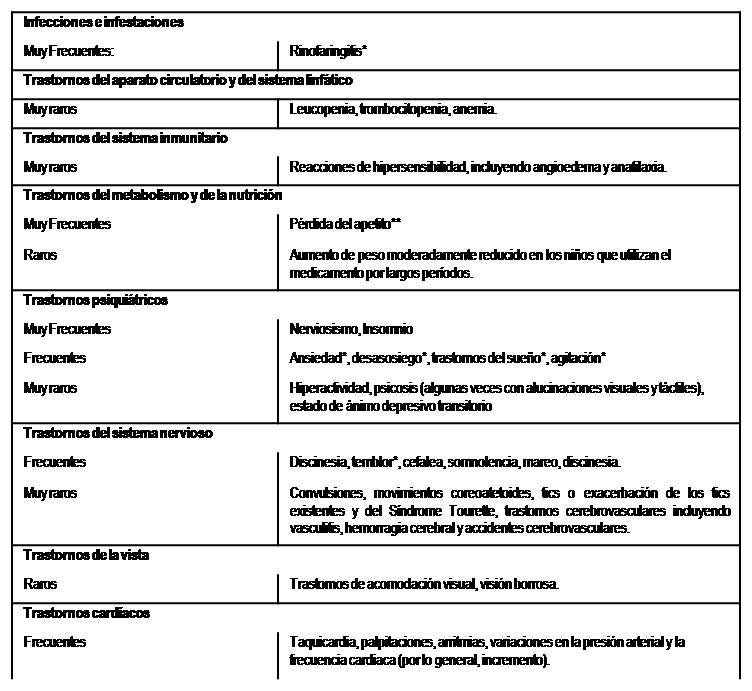
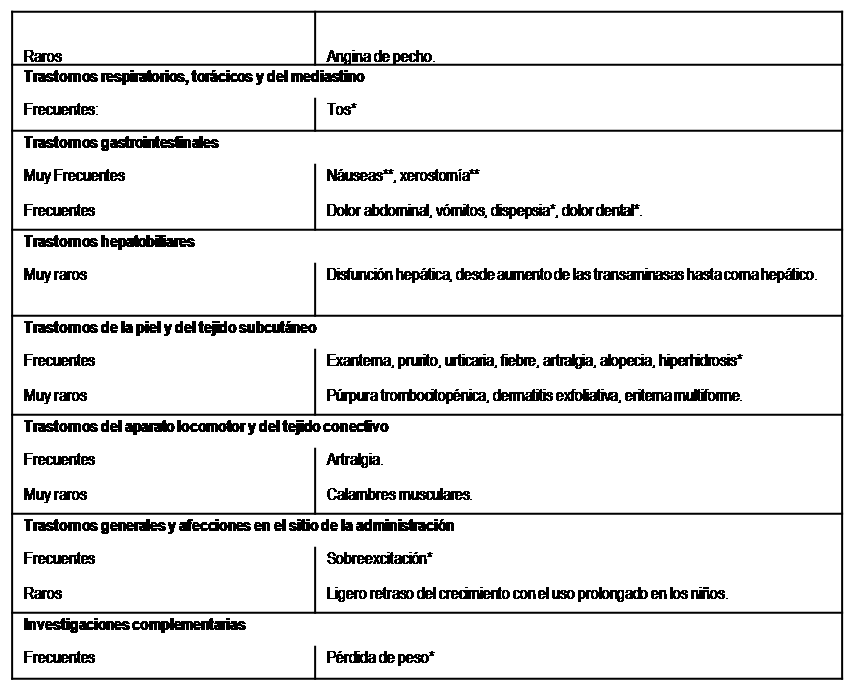
* Reacciones adversas notificadas durante el estudio clínico sobre el tratamiento con Ritalin LA en adultos con TDAH.
** La frecuencia de las reacciones adversas está basada en la frecuencia observada en el estudio clínico sobre TDAH en adultos la cual fue mayor que la cifra registrada anteriormente en niños.
Se han recibido reportes muy raros de Síndrome Neuroléptico Maligno escasamente documentado. La mayoría de estos reportes indican que los pacientes recibían, además, otros medicamentos. Se desconoce el papel que RITALIN® LA haya podido tener en esos casos.Efectos adversos de reportes espontáneos y casos en la literatura (frecuencia desconocida).
Los siguientes efectos adversos han sido derivados de la experiencia post-marketing con RITALIN® vía reportes de casos espontáneos o en la literatura. Debido a que estas reacciones son reportadas voluntariamente por una población de tamaño desconocido, no es posible estimar realmente su frecuencia y por lo tanto se categorizan como de frecuencia desconocida. Las reacciones adversas por clases de trastornos del diccionario MedDRA (por sistema u órgano). En cada clase de trastornos, las reacciones adversas se han clasificado en orden decreciente de frecuencia, y en cada categoría de frecuencia se han clasificado en orden decreciente de gravedad.
Tabla 2. Efectos adversos de reportes espontáneos y casos en la literatura (frecuencia desconocida).

Efectos adversos adicionales que se han reportado en el uso de productos que contienen metilfenidato.
La lista de abajo muestra reacciones adversas no mostradas para RITALIN® LA (vea la tabla 4) que han sido reportadas con otros productos que contienen metilfenidato, basados en datos de estudios clínicos y reportes espontáneos posterior a la comercialización del medicamento.
Trastornos hematológicos y linfáticos: Pancitopenia
Trastornos del sistema inmunológico: Reacciones de hipersensibilidad, como hinchazón del pabellón auditivo.
Trastornos psiquiátricos: Irritabilidad, agresividad, labilidad emocional, comportamiento anormal o de pensamiento, ira, planificación o intento de suicidio (incluyendo el suicidio), estado de ánimo alterado, cambios de humor, estado de alerta aumentado, manías, desorientación, afectación en la libido, apatía, comportamiento repetitivo, sobre concentración, estado confuso, dependencia, se han descrito casos de abuso y dependencia frecuentemente en formulaciones de liberación inmediata.
Trastornos del sistema nervioso: Déficit neurológico isquémico reversible, migraña.
Trastornos de la vista: Diplopía, midriasis, alteración de la visión.
Trastornos cardiacos: Paro cardiaco, infarto al miocardio.
Trastornos vasculares: Frialdad periférica, fenómeno de Raynaud.
Trastornos respiratorios, torácicos y mediastínicos: Dolor faringo-laríngeo, disnea.
Trastornos gastrointestinales: Diarrea, estreñimiento.
Trastornos de la piel y tejido subcutáneo: Edema angioneurótico, eritema, eritema fijo pigmentario.
Trastornos del aparato locomotor y del tejido conectivo: Mialgia, espasmos musculares.
Trastornos renales y urinarios: Hematuria.
Trastornos mamarios y del sistema reproductor: Ginecomastia.
Trastornos generales y afecciones en el sitio de la administración: Dolor de pecho, fatiga, muerte súbita de origen cardiaco.
Exploraciones complementarias: Soplo cardiaco.
Caja de cartón con frasco PEAD etiquetado con 30 ó 60 cápsulas de liberación prolongada con 10 mg ó 20 mg ó 30 mg ó 40 mg.
DOSIS
Generalidades
La dosis de RITALIN® LA debe adaptarse a las necesidades y respuestas clínicas de cada paciente.
En el tratamiento del TDAH, se procurará que la administración del medicamento coincida con los períodos de mayor estrés escolar, conductual ó social.
El tratamiento con RITALIN® LA debe comenzar con una dosis reducida, con incrementos semanales. No se recomiendan dosis diarias superiores a 60 mg en el tratamiento de la TDAH en niños.
En adultos no se recomienda administrar dosis diarias superiores a 80 mg para el tratamiento del TDAH.
Si los síntomas no mejoran con el aumento gradual de la dosis a lo largo de un mes, debe interrumpirse la administración del medicamento.
Si los síntomas empeoran o sobrevienen otras reacciones adversas, se debe reducir la dosis o, si fuera preciso, interrumpir la administración del medicamento.
Evaluación previa al tratamiento
Antes de comenzar el tratamiento con RITALIN® LA, se debe evaluar a los pacientes para descartar la existencia de trastornos cardiovasculares y psiquiátricos preexistentes, así como de antecedentes familiares de muerte súbita, arritmia ventricular y trastornos psiquiátricos. (ver CONTRAINDICACIONES Y PRECAUCIONES GENERALES).
Evaluación periódica del tratamiento del TDAH
No es necesario prolongar indefinidamente el tratamiento farmacológico. El médico debe valorarlo periódicamente y probar periodos sin medicación para determinar cómo evoluciona el estado del paciente sin farmacoterapia. La mejoría puede persistir tras la suspensión temporal o definitiva del medicamento.
En el TDAH infantil, por lo general, el tratamiento puede suspenderse durante la pubertad o después de ésta.
TDAH
Niños y adolescentes (a partir de los 6 años de edad)
RITALIN® LA se administra por vía oral una vez al día, por la mañana. La dosis inicial recomendada de RITALIN® LA es de 20 mg. Cuando el médico considere que es conveniente administrar una dosis inicial menor, los pacientes pueden comenzar el tratamiento con una dosis de 10 mg.
La dosis diaria máxima que no debe sobrepasarse es de 60 mg.
Adultos
En adultos, RITALIN® LA es la única formulación adecuada para el tratamiento del TDAH. RITALIN® LA se administra una vez al día.
Pacientes no tratados anteriormente con metilfenidato (ver FARMACOCINÉTICA Y FARMACODINAMIA): la dosis inicial recomendada de RITALIN® LA en pacientes que no están tomando metilfenidato es de 20 mg una vez al día.
Pacientes que ya están tomando metilfenidato: el tratamiento puede continuar con la misma dosis diaria. Si el paciente recibía la formulación de liberación inmediata, debe cambiar a la dosis recomendada adecuada de RITALIN® LA (ver mas adelante “Cambio del tratamiento del paciente a RITALIN® LA”).
La dosis diaria máxima que no debe sobrepasarse es de 80 mg. Se recomiendan las mismas dosis para mujeres y varones adultos. Cambio del tratamiento del paciente a RITALIN® LA
La dosis recomendada de RITALIN® LA es igual a la dosis diaria total de la formulación de liberación inmediata, sin sobrepasar una dosis total de 60 mg en niños y de 80 mg en adultos. La siguiente tabla muestra un ejemplo que ilustra el caso de pacientes que pasan de la formulación de liberación inmediata o de liberación sostenida a RITALIN® LA.
Tabla 2 Dosis diaria recomendada cuando se cambia el tratamiento de los pacientes por RITALIN® LA.
|
Dosis previa de Metilfenidato |
Dosis recomendada de RITALIN® LA |
|
5 mg de metilfenidato dos veces al día |
10 mg una vez al día |
|
10 mg de metilfenidato dos veces al día o 20 mg de metilfenidato SR una vez al día |
20 mg una vez al día |
|
15 mg de metilfenidato dos veces al día |
30 mg una vez al día |
|
20 mg de metilfenidato dos veces al día o 40 mg de metilfenidato SR una vez al día |
40 mg una vez al día |
Respecto a otros tratamientos con metilfenidato, la dosis inicial se elegirá con criterio clínico. Si fuera necesario el ajuste posológico, se puede aumentar la dosis de RITALIN® LA a razón de 10 mg por semana en los niños y de 20 mg por semana en los adultos.
Poblaciones Especiales Insuficiencia Renal
No se han realizado estudios en pacientes con insuficiencia renal (ver FARMACOCINÉTICA Y FARMACODINAMIA).
Insuficiencia Hepática
No se han realizado estudios en pacientes con insuficiencia hepática (ver FARMACOCINÉTICA Y FARMACODINAMIA).
Pacientes Geriátricos
No se han realizado estudios en pacientes mayores de 60 años de edad (ver FARMACOCINÉTICA Y FARMACODINAMIA).
VÍA DE ADMINISTRACIÓN: Oral.
Método de administración
Las cápsulas o el contenido de las cápsulas de RITALIN® LA no se deben triturar, masticar ni fragmentar. Las cápsulas de RITALIN® LA pueden administrarse con o sin alimentos. Se pueden ingerir enteras o, alternativamente, se puede esparcir su contenido sobre una pequeña porción de alimento (véanse las instrucciones específicas a continuación).
Administración de RITALIN® LA por esparcimiento del contenido de la cápsula sobre la comida
Las cápsulas se pueden abrir con cuidado y los microgránulos del interior pueden esparcirse sobre un alimento blando (por ejemplo, puré de manzana). No debe calentarse el alimento porque ello afectaría las propiedades de liberación modificada de esta formulación. La mezcla de fármaco y alimento debe consumirse de inmediato y en su totalidad. Esta mezcla no puede guardarse para consumo posterior.
Una única dosis de RITALIN® LA facilita una exposición global al metilfenidato (ABC) equiparable a la que se obtiene con la misma dosis total de los comprimidos de RITALIN® administrados dos veces al día.


